


ICH Q7A 对于原料药(Active Pharmaceutical Ingredient, API)的定义:任何旨在供生产一种药物制剂,并作为其活性成分的物质或混合物,这类物质旨在疾病的诊断、治疗、缓减、处置和预防及影响人体的结构和功能等方面发挥药理作用或其他的直接效益。01原料药控制策略-有机杂质根据原料药的合成工艺

分析方法在药学质量研究中扮演重要的角色,普析手段目前还是在分析领域占据重要的位置,一般尤以HPLC-UV占比最大,一个好的分析方法能有效检出样品中存在的所有杂质,不遗漏某些杂质的检出,以免误导工艺人员正确的开发。 分析方法的建立往往在原
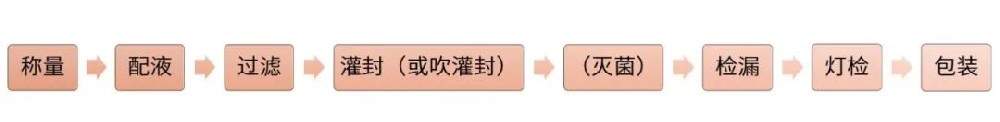
滴眼剂系指由原料药物与适宜辅料制成的供滴入眼内的无菌液体制剂,其生产和质量要求一般参考注射剂的技术要求。本文结合《化学药品注射剂仿制药质量和疗效一致性评价技术要求》等相关要求,具体阐述滴眼液研究过程中的研发内容及注意事项。参比制剂信息确认参比制剂来源确

根据国家相关法律法规要求,药品上市许可持有人(申请人)应当主动开展药品上市后研究,实现药品全生命周期管理。鼓励持有人运用新生产技术、新方法、新设备、新科技成果,不断改进和优化生产工艺,持续提高药品质量,提升药品安全性、有效性和质量可控性。但药品上市后变更不得对药品的安全性、有效性和质量可控性产生不良

摘要:药物中N-亚硝胺杂质的检测以及最近出现的亚硝胺类原料药相关杂质(NDSRIs)给药品制造商和监管机构都带来了巨大挑战。NDSRIs主要与药品中发生的反应有关,这带来了特殊的复杂性。本文将探讨围绕这些杂质形成的现有技术知识,包括风险因素、反应条件和潜在的控制策略。对这些领域的科学理解仍在不断发展,我们将既强调

摘要:水溶性差的药物越来越普遍,这突显了对有效制剂策略的需求,无定形固体分散体(ASD)为提高溶解度和生物利用度提供了一种有前景的解决方案。本综述整合了现有知识,研究了关键进展,并对该领域提供了广泛而结构良好的视角。它探讨了药物的物理化学性质及其对制剂策略的影响,考察了聚合物在维持过饱和和抑制结晶方面的

核心研究“四维框架”:全面评估变更影响安全性(Safety):确保包材自身无害,不引入新风险;保护性(Protectiveness):验证包材能否有效保护药品;功能性(Functionality):考察包材是否适用、易用;相容性(Compatibility):研究药品与包材的相互作用;变更研究的“落地执行”:等同性/可替代性评价与申报综合评估与等

国家药品监督管理局药品审评中心《化学仿制药药学研究重大缺陷(试行)(征求意见稿)》(2025年12月3日发布)中要求:不同申请的申报资料共用研究数据(包括但不限于原辅包研究、处方开发、工艺开发、工艺验证、质量研究、对照品研究、相容性研究、稳定性研究等的研究数据)的,包括新申报的药品与已批准药品共用研究数据的

质量分析控制相关问题问题16:新药研发过程中,代谢产物结构发现有警示结构,实际生产和稳定性研究中没有产生,那这个代谢产物也要按照ICH M7研究吗?答:要明确一下,如果这个代谢产物在样品实际生产和稳定性放置过程中不会产生,就不属于药学研究的部分。这个代谢产物会是临床用药需要考虑的问题。更多的要从结合临床风险/

质量分析控制相关问题问题1:申报IND时,对GMP批次的要求是什么?答:GMP批次是不是必须申报?刚才我们老师已经讲过,就是申报IND时,临床实行的是默认许可60天,大家能够预计到临床默认许可的时间,所以建议申报GMP批次,但不是必须。为什么会这样建议?我们认为这是一个安全性的风险考量。我们发现,有一些申报案例如

制剂工艺相关问题问题1:常见IND申报时,要做剂量探索,剂量也没有确定,药物处于研发早期,为了节约研发经费、节约时间、避免浪费,是不是可以采取灵活的制剂形式申报?答:这个做法其实是国际通行的。最简单的国际通行做法是国外申请人有直接拿原料药装胶囊。这种做法我们也是接受的。各公司应根据自己的研发成本和进度考虑

在天然产物和药物分子的世界里,吲哚是当之无愧的 “明星骨架” — 从抗癌药物到抗菌试剂,从植物激素到生物活性分子,它的身影无处不在。因此,如何高效地给吲哚 “加装” 不同的功能基团,一直是有机化学领域的研究热点。长期以来,这个研究面临一个棘手的 “痛点”:吲哚有两个关键反应位点(N1 位和 C3 位),传统方法要

研发过程中遇到的问题解答1、 在制定质量标准时,产品未检出某些合成过程中用到的溶剂,那么我们如何提供足够的数据证明它呢?是检测连续3批样品,报告检测结果与定量限便足够了吗?答:是的。用验证过的方法检测3批样品,报告检测结果与定量限。2、 关于参照USP/EP建立产品质量标准鉴别项时,USP/EP鉴别项可能有4-5种鉴别方

开篇引言世界著名作家、大思想家斯宾塞·约翰逊曾经说过“唯一不变的是变化本身”,而在药物研发过程中,药物活性成分的合成往往伴随着杂质的生成,任何物质的纯净程度只能无限接近100%,在人类认知的范围内目前还不存在100%纯净的物质,换句话说“认知中可以存在的纯净物质那只有不纯物了”。1 药物杂质与基因毒性杂质介绍

药物毒理学是一门研究药物对机体不良或有害作用的学科。一方面,它探究药物的毒性效应及其与分子结构之间的关系;另一方面,研究药物在体内的吸收、分布、代谢和排泄过程及其规律,并阐明机体防御体系对药物毒性的影响。调查显示,在候选药物的临床前阶段,毒性问题是开发失败的主要原因之一,约

针对目前国内化学药品复方制剂研究中存在有关物质研究方法的不规范和限度确定的不合理, 本文建议在复方制剂的有关物质研究中, 对各主成分的有关物质进行分别研究和控制, 并对复方制剂中有关物质定性归属的几种研究方法进

摘要本研究报告旨在深入探讨一个在药品研发与生产中至关重要的问题:当相容性实验或元素分析过程初步显示某种元素的浓度可能超过ICH Q3D指南设定的允许每日暴露量(Permitted Daily Exposure, PDE)时,是否可以以及如何利用ICH Q3D培训模块2(Module 2: Justification for Exceeding a PDE)进行后续的风险再评估,以论证检

1小分子化合物进行结构确证的一般顺序单一组分化合物通常是定向合成、天然产物提取、发酵提取或半制备等方式制备得到,通过液相或气相等检测手段评估纯度(原料药纯度通常≥99.0%;杂质纯度通常≥90.0%)后,主要通过核磁共振氢谱(1H-NMR)、光谱及常规质谱(MS)等方法,基于合成机理推断平面结构;如合成机理不明确,采用

适用于化学药品注射剂生产过程中直接接触液体的管路类、滤器类、密封件类、配液袋类等塑料组件系统。考虑到接触时间短、相容性风险低,用于称量、转移、配料的辅助类塑料组件系统通常不在本指南范围内,但若经分析存在风险,亦可参照本指南进行研究。制剂申请人作为责任主体,应基于风险评估及必要的相容性研究,确认化学药

最近,国际人用药品注册技术要求协调会(ICH)发布了Q3E指南(可提取物与浸出物指导原则)Step2草案,面向全球公开征求意见。这份指南预计2027年6月正式落地(Step4阶段),一旦实施,将直接影响药企的药品研发、生产、包装全流程——毕竟,可提取物(Extractables)和浸出物(Leachables)这两

摘要 汉森溶解度参数(Hansen Solubility Parameters, HSP)作为一种强大的半经验性理论工具,通过将物质的内聚能密度分解为色散力(dD)、极性力(dP)和氢键力(dH)三个维度,实现了对“相似相溶”原理的精确定量化。在日益追求精准、高效和绿色的化工、制药及化妆品行业中,HSP不仅彻底改变了

在药品开发与质量控制领域,可提取物(Extractables, E)与可浸出物(Leachables, L)的相关性(Correlation)是ICH Q3E指南的核心科学概念之一。用户问题中提到的“扫描研究”,在E&L评估的语境下,通常指的是采用非目标性分析(Non-Targeted Analysis)&nb

在药品共线生产的质量控制中,每日允许暴露量PDE是衡量交叉污染风险、设定清洁限值的黄金标准。然而,一个常见却令人困惑的现象是:针对同一个药物,不同专家计算得到的PDE值往往不一致。这并非计算错误,而是科学评估中专家判断的体现。行业普遍接受PDE值在3倍以内的差异属正常,甚至3到10倍的差距,在某些情况下也是合理的

在药品研发、生产及质量控制领域,杂质分离和鉴定是保障产品安全性、有效性和质量稳定性的核心环节。随着现代制药工业向高纯度、高活性、复杂结构方向发展,药物中可能存在的杂质类型日益多样化,包括合成工艺引入的中间体、副产物、残留溶剂,储存过程中产生的降解产物,以及包装材料迁移的

根据ICH Q3E草案指南,Leachables-Extractables Correlation(浸出物-可提取物相关性)是药品包装和给药系统质量风险管理的重要组成部分。以下是该内容的主要要点:主要内容概述1.相关性评估目的:建立浸出物(leachables)与可提取物(extractables)之间的定性和定量关系,用于识别潜在风险并支持质量控制策略。2.相关性建立条