

α- 重氮酮底物的制备方法有以下几种:
Wolff重排反应具有如下几个特征:
反应机理
可能的有两种机理,一种是先裂解生卡宾,再重排:
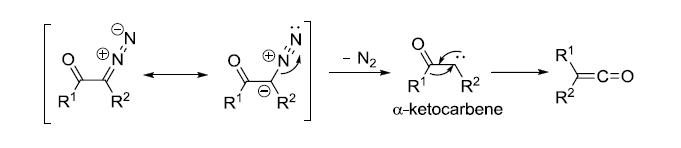
另一种是整个过程协同进行:

对于空间受阻的底物,银离子催化失败,表明必须与离子形成底物络合物。在这些情况下,光化学激发是选择的方法。
溶剂会影响反应过程。如果在甲醇中作为溶剂进行Wolff重排,则从O-H插入点到卡宾中间体的副产物的出现:

反应的过程和迁移偏好可取决于反应的条件(热,光化学,金属离子催化)。如果R是苯基,则主要产物来自重排,而甲基给出更多的插入副产物。
2-重氮-1,3-二酮的反应也有助于确定迁移能力:

在光解中,优选甲基用于重排,而在热解条件下,苯基取代基优先迁移。氢总是超过苯基的迁移能力。芳基或2-重氮酮基羧酸烷基酯中的烷氧基从不迁移。
反应实例

陆德维希·沃尔夫在1912年发现,α-重氮酮在加热、光照或者过渡金属催化的条件下消除氮气,形成卡宾之后进行重排得到烯酮的反应称为Wolff 重排。

烯酮作为中间产物,可以被弱酸性亲核体进攻,可以和水反应制备羧酸,和醇反应制备酯,和胺反应制备酰胺,发生Staudinger烯酮环加成合成各种四元环化合物。可以和烯烃,醛酮和亚胺进行[2 + 2]环加成得到环丁酮,β -内酯和β -内酰胺。

免责声明:本站提供的一切文章和内容信息仅限用于学习和研究目的;不得将上述内容用于商业或者非法用途,否则,一切后果请用户自负。本站信息来自网络收集整理,版权争议与本站无关。我们非常重视版权问题,如有侵权请邮件与我们联系处理。敬请谅解!
本文最后更新于2023-11-22 10:28:35,如果你的问题还没有解决,可以加入交流群和群友们一起讨论。